Tenside
Nach einem Vorschlag von E. Götte (1964) von lat. tensio=Spannung abgeleitete
Bezeichnung für Substanzen, die die Grenzflächenspannung herabsetzen. Tenside
verfügen über einen charakteristischen Aufbau und weisen mindestens eine
hydrophile und eine hydrophobe funktionelle Gruppe auf.
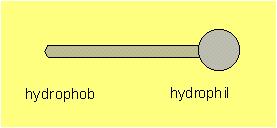
Abb. 1 charakteristischer Aufbau eines Tensids
Bei den hydrophilen Anteilen des Moleküls handelt es sich
meist um polare funktionelle Gruppen, während die hydrophoben Teile in der Regel
unpolare Kohlenwasserstoff-Reste darstellen. Löst man eine derartig aufgebaute
Substanz in Wasser, so wird sie sich, sofern der hydrophile Teil überwiegt,
lösen; überwiegt hingegen der hydrophobe Rest wird man ein Aufrahmen beobachten.
Erst wenn beide Teile des Moleküls im Gleichgewicht zueinander stehen, wird sich
die Substanz an der Grenzfläche anreichern und ausrichten, d.h. hydrophile
Gruppen weisen in die wässrige Phase, hydrophobe Gruppen in Richtung der anderen
festen, flüssigen oder gasf. Phase. Dieses Verhalten ist typisch für Tenside und
unterscheidet sie von anderen Stoffen.
Löst man z.B. das Salz der Essigsäure
in Wasser, liegen unabhängig von der Konzentration diskrete Molekül bzw.
Molekül-Ionen vor, während sich die Natriumstearat-Moleküle zunächst an der
Oberfläche der Lsg. anreichern, bis diese vollständig bedeckt ist. Bei einer
weiter zunehmenden Konz. bilden sich höhere Aggregate, sog. Micellen, bei denen
sich die Tensid-Mol. dergestalt anordnen, daß die polaren Gruppen eine
Kugelschale bilden. Die Fähigkeit zur Micellisierung unterscheidet Tenside
ebenfalls von allen übrigen org. Stoffen und ist die Voraussetzung für das
Vermögen von Tenside, Unlösliches löslich zu machen.
Histor.: Die
Sumerer (um 2500 v.Chr.) gaben in ihren Keilschriften als erste davon
Kenntnis, daß sie aus Holzasche und Öl eine seifenähnliche Substanz herstellten.
Bei den Aufzeichnungen handelt es sich um Angaben zum Waschen und Walken von
Wollstoffen. Nach Plinius war auch den Ägyptern, Galliern u. Germanen die
Herstellung von verseiften Fetten und Ölen bekannt. Solche Produkte dienten
jedoch weniger zum Waschen, sondern zu kosmetischen Zwecken oder als Heilmittel.
Erst der in Rom praktizierende griechische Arzt Claudius Galenos
(131–201 n.Chr.) machte auf die Reinigungswirkung der Seife aufmerksam,
obgleich Ausgrabungen in Pompeij zeigen, daß dort schon 79 v. Chr. Seife
hergestellt wurde. Überlieferungen aus dem Mittelalter zur Seife und ihrem
Gebrauch sind spärlich.
Man weiß, daß Karl der Große im fränkischen Reich
das Handwerk der Seifensieder förderte. Araber, Spanier, Italiener und Franzosen
brachten später, dank der Rohstoffquelle Ölbaum, die Seifensiederei zur Blüte.
Die Entwicklung einer Seifensiederzunft in Deutschland ist jedoch erst für die
Zeit ab dem 14. Jh. belegt. Im 17. und 18. Jh. stieg der Bedarf an
Pottasche und Pflanzenasche für die Glas- und Seifen-Herst. so stark an, daß ein
ernster Raubbau an Bäumen u. Pflanzen einsetzte. In ihrem Bemühen, eine weitere
Zerstörung der Natur zu verhindern, setzte 1775 die französische Akademie der
Wissenschaften einen Preis für die synthetische Herstellung von Soda aus,
welcher Leblanc zugesprochen wurde. Seit der Leblanc-Seifenfabrikation 1791
konnte Seife besser und preiswerter hergestellt werden und avancierte vom Luxus-
zum Gebrauchsgegenstand. 1823 berichtete Chevreul über die „wahre Natur des
Verseifungsprozesses“ und legte damit die wissenschaftliche Basis für die
Tensidchemie.
Mit dem Beginn des 20. Jh. und der Einführung der
„selbsttätigen“ Waschmittel wurde die Seife in Mehrkomponentensystemen zum
Reinigen von Textilien mitverwendet, wobei sie mit Buildern (Soda, Wasserglas,
Perborat) kombiniert wurde. Im Jahre 1907 wurde von HENKEL das Markenprodukt
„Persil®“ eingeführt: „Per“ wie Perborat, „Sil“ wie Silicat. Diese Waschmittel
ersparten der Hausfrau die langwierige, wetterabhängige Rasenbleiche und
brachten durch ein höheres Waschvermögen auch Erleichterungen bei der
Handwäsche. Etwa zur gleichen Zeit führte der Fortschritt der technischen
Entwicklung zum Übergang von der Handwäsche zur Maschinenwäsche, womit eine
Änderung der Zusammensetzung von Waschmitteln und eine Abstimmung auf die neue
Technologie erforderlich wurde. Dabei zeigte sich, daß Seife den gravierenden
Nachteil der Härteempfindlichkeit besitzt, also mit den Härtbildnern des Wassers
unlösliche Calcium- od. Magnesium-Salze bildet, die zu einer Verringerung der
Waschkraft und zu Inkrustierungen im Gewebe führen. Damit begann die Suche nach
anderen Waschrohstoffen, die den geänderten Anforderungen Rechnung trugen.
Als Vorläufer der modernen synthetischen Tenside kann das Türkischrotöl
angesehen werden, das bei der Herstellung der beliebten Inlettfarbe Türkischrot
als Egalisiermittel angewendet wurde. Türkischrotöle stellten zunächst
Emulsionen ranziger Öle aus den Rückständen der Olivenöl-Gewinnung dar, die auch
als Tournantöle bezeichnet und mit Soda, Wasser u. Schafsmist emulgiert wurden.
1834 wurde von Runge erstmals ein sulfoniertes Öl durch Einwirkung von
Schwefelsäure auf Olivenöl hergestellt, das von der Elsässer Druckerei
Wesserling für Alizarin-gefärbte Beizendruckartikel eingesetzt wurde. Das
Verfahren gelangte vom Elsaß aus nach Schottland, wo anstelle von Olivenöl das –
damals – billigere Rizinusöl eingesetzt wurde. Dies war die Geburtsstunde des
Sulfo-ricinolats, das bis in die heutige Zeit Anw. als Netzmittel in der
Baumwollfärberei findet.
Im Jahre 1917 gelang dem deutschen Chemiker
Fritz Günter bei der BASF die erste Alkylierung und Sulfonierung des
Naphthalins. Das dabei erhaltene Alkylnaphthalinsulfonat zeigte zwar ein starkes
Netzvermögen und einen beständigen Schaum, war jedoch nicht waschaktiv. Erst
später erkannte man, daß dies auf die Wahl eines zu kurzen Alkyl-Restes
zurückzuführen war.
Die eigentliche Entwicklung moderner Tenside hat in den
zwanziger Jahren des letztens Jahrhunderts ihren Anfang genommen. Auf der Suche
nach besseren Textil- und Färbereihilfsmitteln sulfonierte Bertsch bei der
Böhme-Chemie in Chemnitz Ricinolsäure sowie deren Ester und entwickelte dabei
ein Ricinolsäurebutylestersulfonat, das zwar gute netzende Eigenschaften, jedoch
ebenfalls nur ein geringes Waschvermögen besaß. Bei der Untersuchung der
Sulfierung von Fettalkoholen stieß Bertsch schließlich auf die herausragenden
Tensid-Eigenschaften des Natriumdodecylsulfats. An eine industrielle Verwertung
war indes noch nicht zu denken, da Fettalkohole bis zu diesem Zeitpunkt durch
Reduktion von Fettsäuren mit Natrium nach dem Verfahren von Bouveault und Blanc
hergestellt werden mußten. Im Jahre 1928 jedoch – also beinahe zur gleichen Zeit
– war von Schrauth bei der Deutsche Hydrierwerke AG, der DEHYDAG, in Rodleben
(Sachsen-Anhalt) die katalytische Hochdruckhydrierung von Fettsäureestern zu
Fettalkoholen entwickelt worden. Neben der Hydrierung von Spermöl zu
Stearylalkohol (1-Octadecanol) u. Oleylalkohol (9-Octadecen-1-ol) wurden bald
auch Lauryl (1-Dodecanol) und Myristylalkohol (1-Tetradecanol) hergestellt, so
daß der Weg zur industriellen Herstellung von Fettalkoholsulfaten (FAS)
beschritten werden konnte. FAS wurden erstmals 1932 in Deutschland von HENKEL
(Fewa®) bzw. in den USA von Procter & Gamble (Dreft®) eingesetzt.
Von
Schöller und Wittwer wurden zu Beginn der 30er Jahre des 20. Jahrhunderts bei
der IG Farben erstmals Anlagerungsprodukte von Ethylenoxid an Fettalkohole und
somit die ersten nichtionischen Tenside erhalten. Bei den Leuna-Werken in
Halle-Merseburg wurden Anfang der 40er Jahre von Asinger sek. Alkansulfonate
(SAS) durch photochemische Sulfochlorierung und Fischer-Tropsch-Synthese
erstmals großtechnisch hergestellt.
Die Entwicklung der
Alkylbenzolsulfonate (ABS) geht auf die Feststellung des britischen Chemikers
Adam zurück, daß man aus Hexadecyl- und Octadecylbenzolen nach Sulfonierung und
Neutralisation wasserlösliche Produkte gewinnen kann, die seifenähnlichen
Charakter haben. In den 50er Jahren des 20. Jahrhunderts wurde daraufhin das
Tetrapropylenbenzolsulfonat (TPS) entwickelt, das 1959 bereits 65% des gesamten
Bedarfs der westlichen Welt an synthetischen Tensiden deckte. Der heiße Sommer
1959 zeigte dann jedoch auch die Grenzen des TPS in den Ländern auf, deren
Bedarf an synthetischen Waschmitteln während der letzten Jahre sprunghaft
gestiegen war: auf den Flüssen, an Wehren und Schleusen türmten sich gewaltige
Schaumberge. Man erkannte rasch, daß dies eine Folge des verzweigten Aufbaus des
TPS war, der eine unzureichende biologische Abbaubarkeit bedingte. Die nächste
Generation der Alkylbenzolsulfonate zeichnete sich durch eine lineare
Alkyl-Kette aus und erfüllte hinsichtlich ihrer ökologischen rträglichkeit die
bald erlassenen gesetzlichen Bestimmungen, nach denen der Anion-akt. Anteil in
Wasch- u. Reinigungsmitteln unter festgesetzten Prüfbedingungen in der
Kläranlage zu mindestens 80% abbaubar sein muß.
Einteilung: T. werden im
allg. nach Art u. Ladung des hydrophilen Molekül-Anteils klassifiziert. Hierbei
können vier Gruppen unterschieden werden: Aniontenside, Kationtenside,
nichtionische Tenside (Niotenside) und Amphotenside. Anionische Tenside weisen
als funktionelle Gruppen in der Regel Carboxylat-, Sulfat- oder Sulfonat-Gruppen
auf, während Kationtenside beinahe ausschließlich durch das Vorhandensein einer
quartären Ammonium-Gruppe gekennzeichnet sind. Typisch für Niotenside sind
Polyether-Ketten, während ampholytere Tenside sowohl anionische als auch
kationionsiche Gruppen enthalten und sich demnach je nach pH-Wert wie Anion-
oder Kationtenside verhalten.
Verbrauch: Im Verlauf der letzten 10 Jahre
ist der Welttensid-Verbrauch um etwa 20% gestiegen und betrug 1988 etwa
5 Mio. t. Für die Zukunft kann mit einem weiteren Wachstum gerechnet
werden, da die großen Märkte in Indien und China gerade erst erschlossen werden
und flüssige, Hochtensid-haltige Waschmittelformulierungen zunehmend an
Bedeutung gewinnen. Etwa 2/3 des Verbrauches entfallen auf anion., 1/3 auf
nichtionische Tenside, während der Marktanteil kationionischer und
ampholytischer Tenside vergleichweise gering ist.
Für die Zukunft wird
den kationionischen Tensiden eine stagnierende od. sogar rückläufige Entwicklung
vorhergesagt, da sie verschärften Anforderungen an die biologische Abbaubarkeit
nicht ausreichend gerecht werden und zudem ein gewisses
Sensibilisierungspotential aufweisen. Den ampholytischen Tensiden wird infolge
ihrer hohen Herstellkosten auch in absehbarer Zeit nur die Rolle von
Spezialtensiden zukommen. Obschon die Aniontenside, und hierunter v.a. die Seife
und die Alkylbenzolsulfonate, nach wie vor eine Spitzenstellung im
Welt-Tensidverbrauch einnehmen, hat ihre Bedeutung in den letzten 10 Jahren zu
Gunsten der nichtionischer Tenside deutlich abgenommen. Ursache hierfür ist die
geringere Härteempfindlichkeit sowie die vielfach bessere Löslichkeit
nichtionischer Tenside, wie z.B. der Fettalkoholpolyglykolether und der damit
verbundene Vorteil im Waschverhalten bei niedrigen Temperaturen. Die wachsende
Bedeutung nichtionischer Tenside gibt somit das veränderte Waschverhalten der
Verbraucher wieder, die ähnlich wie in den USA verstärkt zu Waschtemp. von 30°
tendieren.
Unter den drei großen Wirtschaftsregionen nimmt die USA mit
einem Anteil von 45% am Welt-Tensidmarkt die Spitzenstellung unter den
Verbraucherländern ein, gefolgt von Westeuropa u. Japan. 1989 betrug der
Tensid-Verbrauch in der BRD ca. 228000 t. Hierbei kamen den Aniontensiden
51%, den Niotensiden 37% u. den Kationtensiden 10% zu. Die größten Einzeltonagen
entfielen auf das Alkylbenzolsulfonat mit 61000 t und die Gruppe der
Fettalkoholethoxylate mit 54000 t.
Produktion: 1990 betrug die
Weltproduktion an Tensiden ca. 4 Mio. t. Hiervon entfielen auf die USA
und Westeuropa jeweils etwa 44%, auf Japan 12%.
Neben der Seife dominiert das
Alkylbenzolsulfonat mit einer Jahresproduktion von ca. 1 Mio. t. über
allen anderen synthetischen Tensiden. Die beiden anderen wichtigen anionischen
Tenside, die Fettalkoholsulfate und -ethersulfate, entsprechen zusammen nur etwa
der Hälfte der Produktion an ABS, was dessen Bedeutung für die Tensidchemie
unterstreicht. Auf dem zweiten Platz finden sich die Fettalkohol- und die
Alkylphenolpolyglykolether, deren Jahresproduktion zusammen etwa 850000 t
beträgt. Aufgrund der ungünstigen biologischen Abbaubarkeit wird auf den Einsatz
von APE in Europa zunehmend verzichtet; in der BRD werden diese Stoffe auf der
Grundlage einer freiwilligen Selbstbeschränkung der Industrie praktisch nicht
mehr eingesetzt. Es kann daher davon ausgegangen werden, daß die APE zu Gunsten
der FAE zunehmend an Bedeutung verlieren werden.
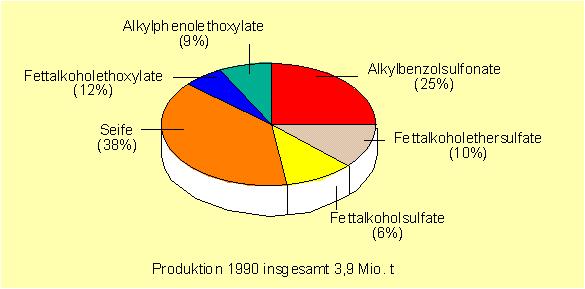
Abb. 2 Welt-Tensidproduktion (1990)
Die sechs aufgeführten T. decken gemeinsam etwa 90 bis 95%
des Tensid-Marktes ab. Von weiterer Bedeutung sind die Ligninsulfonate,
besonders preiswerte Tenside, die durch Sulfitation von Rückständen der
Papierherstellung gewonnen und insbesondere in der tertären Erdölförderung
eingesetzt werden. Weitere typische Aniontenside, wie etwa die Alkansulfonate
oder die a-Olefinsulfonate, besitzen bislang nur eine regionale Bedeutung und
wurden in der Aufstellung nicht berücksichtigt.
Verw.: Das Einsatzgebiet
von T. ist überaus vielfältig (Abb. 4). Den größten Anteil mit fast einem
Drittel besitzt der Textilmarkt, d.h. Anw. die sich auf das Waschen u. Reinigen
von Textilien beziehen. Zweitgrößtes Einsatzgebiet mit 12% sind die kosmet.
Produkte. Hier finden milde T. Einsatz in Schaumbädern u. Haarshampoos u. in
Form von Emulgatoren in Cremes u. Lotionen. Ein gleichgroßes Marktsegment
entfällt auf die Flotation, d.h. das Ausbringen u. Abtrennen von Erzen u.
Mineralien von taubem Gestein.
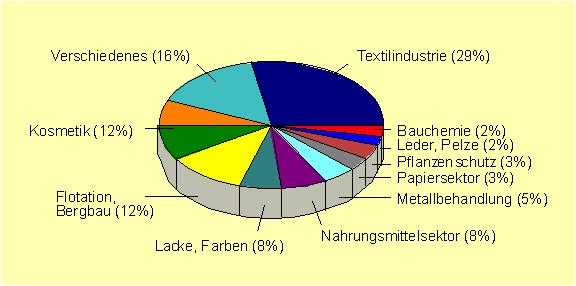
Abb. 3 Einsatz von Tensiden
Weniger bekannt ist, daß Tenside auch auf dem
Nahrungsmittelsektor z.B. in Form der Zuckerester-Emulgatoren unverzichtbare
Hilfsmittel darstellen. Ein gleichgroßes Marktsegment von 8% nehmen die Tenside
im Bereich der Lacke und Farben ein, wo sie ebenfalls als Emulgatoren und
Verdickungsmittel eine große Rolle spielen. Dagegen ist die Bedeutung der
Tenside auf den Sektoren Metallbehandlung, Lederhilfsmittel, Bauchemie und
Pflanzenschutz eher untergeordnet.
Lit.: Chem. Times Trends 7, 38 (1986)
Chem. Unserer Zeit 25, 214 (1991)
Cosm. Toil. 104, 57 (1989)
Fat Sci.
Technol. 92, 49, 287 (1990)
J. Falbe (Hrsg.), „Surfactants in consumer
products“, Berlin: Springer 1986 ï Manuf. Chem. 60, 33 (1989)
Oleagineux 39,
435 (1984)
Parfum. Kosmet. 70, 4 (1989)
Seifen Öle Fette Wachse 116, 251
(1990); 117, 3 (1991)
Soap Cosmet. Chem. Spec. 1988, Nr. 9, 28, 33.
Tenside Surf. Deterg. 24, 70 (1978).
E surface active agents,
surfactants
F agents tensio-actifs, agents de surface, surfactifs
I
tensioattivi
S agentes tensioactivos (de
superficie)
Quelle: CD Römpp Chemie Lexikon – Version
1.0, Stuttgart/New York: Georg Thieme Verlag 1995



